Che differenza c’è tra chemioterapia e target therapy?
All’inizio degli anni ’80, le nuove scoperte nel campo dell’immunologia, della biologia cellulare, e della biologia molecolare hanno permesso ai ricercatori di comprendere meglio i meccanismi molecolari responsabili della trasformazione neoplastica delle cellule.
Di conseguenza sono stati identificati nuovi bersagli molecolari che possano essere colpiti con molecole chimiche o anticorpi monoclonali, che vanno a costituire l’armamentario della target therapy.
Un limite importante della chemioterapia antineoplastica è la sua mancanza di selettività: agendo su bersagli comuni a tutte le cellule, colpisce indiscriminatamente tutte le cellule che si riproducono velocemente, sia neoplastiche (effetto desiderato) sia normali (effetto indesiderato).
La target therapy è invece più selettiva verso il tumore, poiché colpisce bersagli soprattutto, e a volte esclusivamente, espressi dalle cellule tumorali e non da quelle sane, riducendo significativamente gli effetti collaterali.
Conosciamo davvero il cancro?
C’è ancora molto da scoprire sul cancro (ricordiamoci che si tratta di svariate malattie racchiuse sotto lo stesso nome), ma sono stati fatti molti progressi.
Questi hanno portato all’individuazione di alcune caratteristiche chiave di queste patologie: i cosiddetti hallmarks del cancro (Figura). Si tratta di proprietà biologiche assunte dal tumore, che gli permettono di rafforzarsi e sopravvivere. La massa tumorale non è composta esclusivamente da cellule tumorali, ma anche da cellule del sistema immunitario, dei vasi sanguigni e da fibroblasti, cellule sane che il tumore convince a convertirsi alla patologia per aiutarlo a crescere.
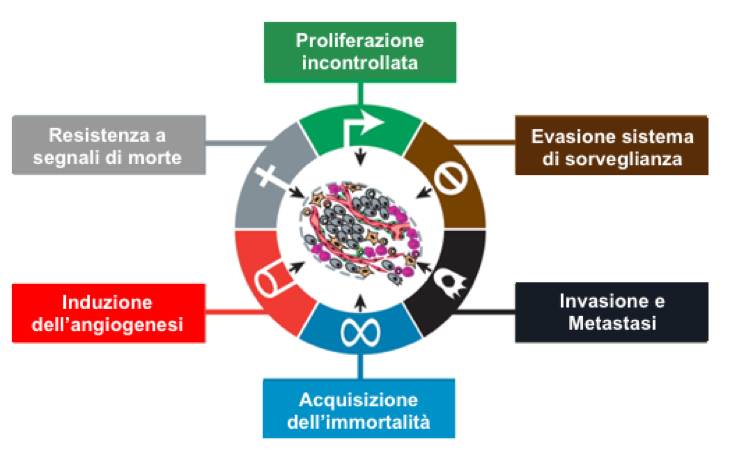
Hallmarks del cancro. Modificata da Hallmarks of Cancer: The Next Generation, doi.org/10.1016/j.cell.2011.02.013
Il tumore, infatti, è in grado di i) proliferare incondizionatamente, senza controllo; ii) sfugge al sistema di difesa, che anzi ad un certo punto si coalizza con esso; iii) richiama a se le cellule dei vasi sanguigni e chiede loro di crearne di nuovi per poter far arrivare ulteriore nutrimento e ossigeno, processo noto con il nome di angiogenesi tumorale; vi) cambia il suo metabolismo, quindi il modo di approvvigionarsi di energia, come già sosteneva il premio Nobel Otto Warburg; v) ed è capace di sfuggire dalla sede primaria per raggiungere e colonizzare altri tessuti, col processo di metastatizzazione.
La ricerca ha permesso di identificare i bersagli molecolari che stanno alla base degli hallmarks, definendo gli oncogeni (cioè i geni che stimolano la cellula a dividersi e proliferare) e gli oncosoppressori (i geni che riducono la crescita cellulare), che se mutati e/o alterati portano allo sviluppo di tumore.
La target therapy delle molecole chimiche
La target therapy interviene sugli oncogeni e sugli oncosoppressori alterati che promuovono lo sviluppo del tumore.
Molti processi all’interno della cellula sono alterati nel cancro, e ciò è dovuto appunto a mutazioni genetiche e alle modifiche delle proteine, che portano alla anormale attivazione di segnali di crescita incontrollata.
Pioniere della terapia bersaglio fu lo sviluppo, agli inizi degli anni ’90, del primo inibitore della proteina tirosina chinasi, imatinib (Glivec®), che venne definito inizialmente il magic bullet, cioè il “proiettile magico” inteso come il farmaco perfetto.
Questo inibitore è in grado di colpire selettivamente una proteina che si forma esclusivamente dalla traslocazione cromosomica che causa la leucemia mieloide cronica, il cromosoma Philadelphia.
Imatinib induceva la remissione nell’80% dei pazienti. Il successo fu tale che altri farmaci vennero generati in grado di colpire selettivamente bersagli iper-espressi dal tumore ma non dalle cellule sane.
Tra questi si annoverano, gefitinib (approvato nel 2001) e lapatinib (nel 2007), inibitori (come dice il nome stesso) del recettore per il fattore di crescita epidermico (EGF), o sunitinib e sorafenib (2009), contro il recettore per il fattore di crescita dell’endotelio vasale (VEGF), in grado di bloccare la formazione dei nuovi vasi richiesta dal tumore (angiogenesi).
Moltissimi altri ancora sono stati immessi in commercio negli anni seguenti, e tutt’ora ve ne sono in sviluppo. Tutti questi farmaci della target therapy sono attualmente usati per il trattamento di diversi tipi di tumore in combinazione con i chemioterapici tradizionali o in combinazione tra loro.
La target therapy degli anticorpi monoclonali
In parallelo, le conoscenze sempre maggiori sulle tecniche del DNA ricombinante e della struttura chimica delle proteine, hanno permesso un’evoluzione anche del concetto di farmaco che non viene più sintetizzato in laboratori chimici ma viene fatto produrre direttamente dalle cellule.
Questi farmaci sono proteine, quindi strutture analoghe a quelle contenute nella cellula, e il più classico degli esempi è l’insulina ricombinante.
Queste procedure hanno aperto le porte alla generazione di anticorpi monoclonali che, ispirandosi agli anticorpi che il nostro corpo è in grado di generare quando deve combattere un microorganismo estraneo, riconoscono con precisione il bersaglio (target) da colpire (epitopo) e lo neutralizzano. Nella target therapy, questi anticorpi sono stati generati contro gli stessi target discussi in precedenza, quindi recettori per fattori di crescita o contro i fattori di crescita stessi.
Qual è stata l’evoluzione degli anticorpi monoclonali?
Il primo farmaco ad azione mirata sviluppato come anticorpo monoclonale contro il meccanismo specifico di azione di un oncogene tumorale (HER2) è stato il trastuzumab, creato nei laboratori della società biotecnologica Genentech, la cui sperimentazione sull'uomo venne avviata nel 1992 e attualmente è impiegato nel tumore al seno Her2 positivo (Leggi anche "Tumore ala seno (o carcinoma mammario): cos'è e quali prospettive ha oggi").
Da qui, oltre 50 anticorpi monoclonali per l’oncologia sono entrati nei trial clinici fino al 20171. Alcuni esempi sono il bevacizumab che neutralizza VEGF ed è impiegato in terapia oncologica, ma anche nella degenerazione maculare (una patologia dell’occhio che porta a cecità) e Rituximab, che invece ha come target la molecola CD20 espresso dalle cellule B del sistema immunitario e quindi impiegato nei linfomi e nelle leucemie che lo iper-esprimono.
Immunoterapia per risvegliare il sistema di sorveglianza
Uno degli hallmarks del cancro è l’evasione da parte del tumore del sistema immunitario di sorveglianza, fino a convincerlo, rilasciando segnali, a collaborare con esso e non attaccarlo più.
Una branca della target therapy, quindi, si occupa di riattivare il sistema immunitario a combattere di nuovo il tumore ed è definita immunoterapia.
Come fa il cancro a ingannare il sistema immunitario?
Il sistema immunitario è capace di distinguere le cellule dell’organismo (self) dalle cellule estranee (non-self).
Per rispettare queste condizioni, l’azione dei linfociti T è mantenuta costantemente sotto il controllo di sofisticati meccanismi, conosciuti come checkpoint immunitari, che determinano quando un linfocita si debba attivare o meno.
Essi consistono in molecole e recettori per queste molecole che vengono espressi dalle cellule cellule T e che servono a placare la risposta immunitaria una volta che è “cessato il pericolo” (ad esempio dopo aver combattuto un’infezione da parte di un microrganismo).
Il tumore approfitta di queste molecole, rilasciandole e ingannando le cellule T che quindi smettono di attaccarlo.
Anticorpi monoclonali come ipilimumab, atezolizumab e nivolumab sono in grado di neutralizzare questi segnali inibitori verso le cellule T, così che queste si riattivino a combattere il tumore.
Questi farmaci hanno avuto, e stanno avendo, enorme successo nel melanoma metastatico ma anche nel tumore al seno triplo negativo2,3.
Riferimenti bibliografici:
1 MAbs. 2020;12(1):1703531. doi: 10.1080/19420862.2019.1703531.
2 N Engl J Med. 2019 Mar 7;380(10):987-988. doi: 10.1056/NEJMc1900150.
3 Lancet Oncol. 2020;21(1):44-59. doi:10.1016/S1470-2045(19)30689-8.
4 Front Pharmacol. 2018;9:1300. doi: 10.3389/fphar.2018.01300.